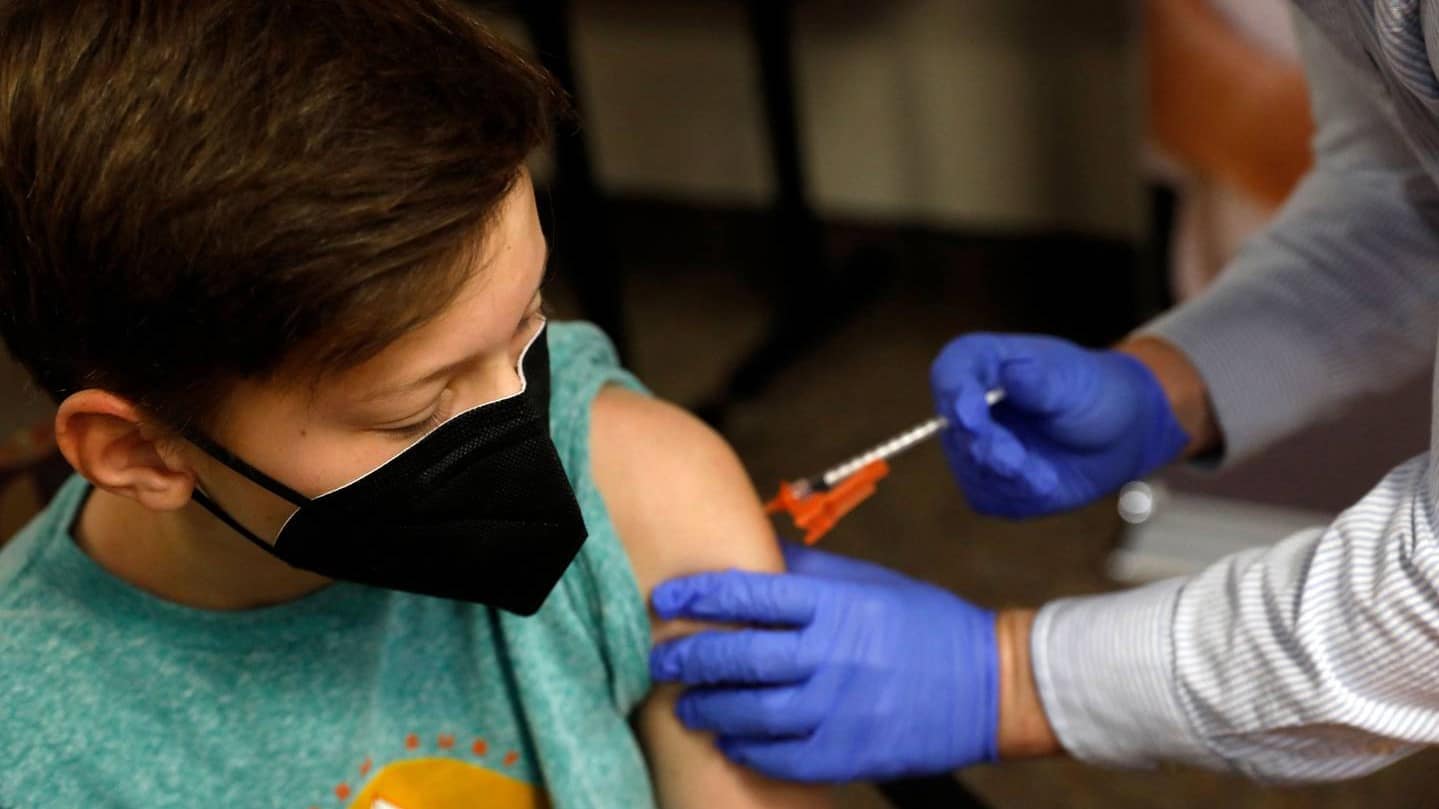
La farmacéutica Moderna afirma que le solicitará a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) que apruebe el uso de emergencia de su vacuna contra la COVID-19 en menores de entre seis meses y seis años de edad, publicó el portal Democracia Ahora.
Moderna sostiene que un ensayo clínico mostró que dos dosis bajas de su vacuna, administradas con un intervalo de cuatro semanas entre una y otra, produjeron una fuerte respuesta inmune en menores de corta edad.